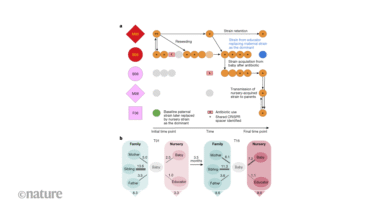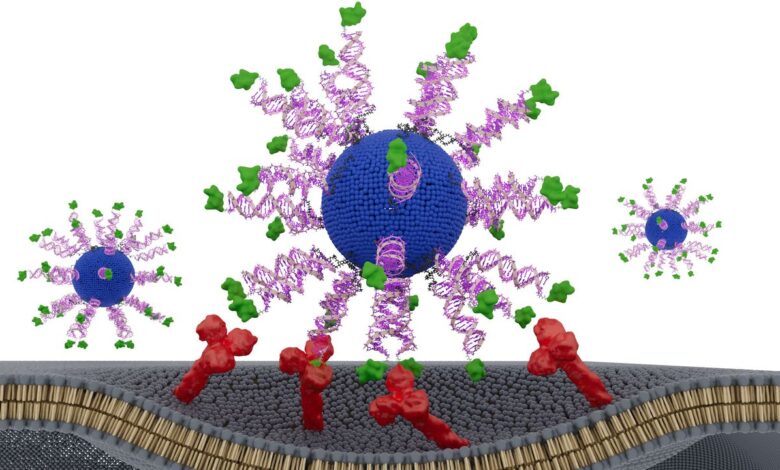
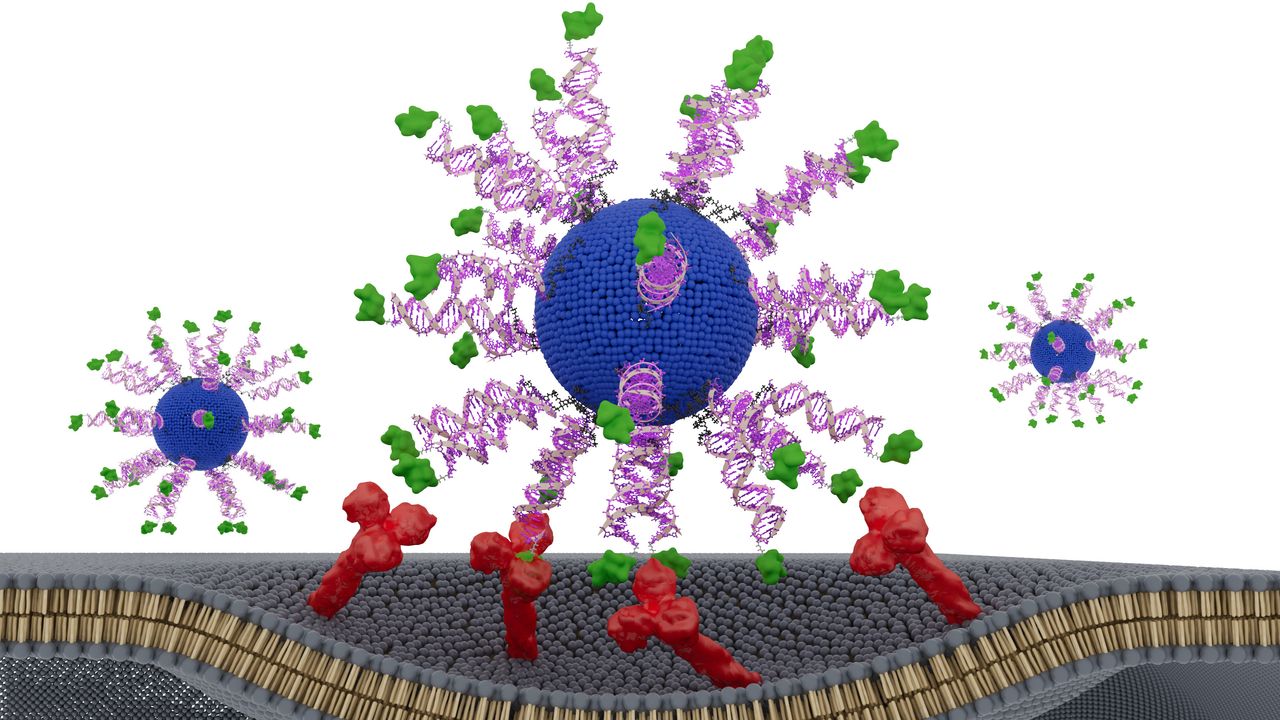
Вакцина дизајнирана за борбу против рака главе и врата изазваног ХПВ-ом показала је обећавајуће резултате у лабораторијској студији на људским ткивима и мишевима.
Ако се покаже делотворним код људи, терапијска ињекција би могла да допуни стандардне терапије рака, а његов дизајн може помоћи научницима да направе боље вакцине за друге болести.
Вакцина Гардасил 9 може спречити ХПВ инфекције и тако смањити ризик од ових карцинома у наставку. Али за људе који већ имају туморе повезане са ХПВ-ом, лечење се и даље ослања на операција, зрачење и хемотерапија. Комбиновање вакцине против рака са овим конвенционалним терапијама могло би да побољша њихову ефикасност учењем имунолошког система да се бори против рака.
Сада су научници конструисали вакцину против рака чије су компоненте распоређене у јединствену структуру. Слично превентивним вакцинама, вакцине против рака обучите имуни систем да препозна специфичне протеине – у овом случају, протеин који се налази на ХПВ-позитивним туморима – и често садрже састојке који се називају адјуванси који појачавају имуни одговор. Међутим, уместо да спрече болест на првом месту, вакцине против рака се генерално користе за лечење болести и спречавање њеног поновног појављивања.
У лабораторијским студијама ХПВ-позитивног карцинома главе и врата, ова нова, пажљиво направљена вакцина успорила је раст тумора и побољшала преживљавање код мишева, према студији објављеној у среду (11. фебруара) у часопису Сциенце Адванцес.
др Езра Коенспецијалиста за рак главе и врата у УЦ Сан Диего Хеалтх који није био укључен у студију, рекао је да ако вакцина делује на људима, може да допуни стандардне терапије.
„Може се замислити мултимодални приступ како би се пацијент ослободио болести, а затим вакцина како би се спречило понављање“, рекао је он. Али он је упозорио да се резултати лабораторијских животиња и изолованих ткива не преносе увек на људе. „Прави тест је у људима“, рекао је он за Ливе Сциенце у мејлу. „Али снажни претклинички подаци, попут ових, повећавају шансе за успех у клиничким испитивањима.“
У овом случају, приметан је основни дизајн вакцине.
„Кључни налаз је да структура вакцине чини значајну разлику“, рекао је Коен. „Успешна вакцинација није само одабир тачних антигена (циљних протеина), већ и постављање тих антигена у праву секвенцу са другим елементима вакцине.
Вакцина користи сферичне нуклеинске киселине (СНА) — ДНК честице у облику кугле које улазе у имуне ћелије и везују се за мете ефикасније од линеарне ДНК ради. Свака СНА наночестица унутар вакцине састоји се од масног језгра окруженог адјувансом и фрагмента ХПВ протеина из туморских ћелија. Адјуванс имитира бактеријску ДНК и имуни систем га препознаје као „страно“.
Истраживачи су тестирали три дизајна, мењајући само начин на који је ХПВ фрагмент био позициониран. Једна верзија га је сакрила унутар наночестице, док су друге две верзије имале ХПВ фрагмент на површини честице, причвршћен на различитим крајевима структуре фрагмента, познат као Н крај и Ц крај.
Верзија са фрагментом причвршћеним за површину преко његовог Н краја изазвала је најјачи имуни одговор, открио је тим. Овај дизајн је навео Т ћелије убице – имуне ћелије које уништавају заражене, оштећене и канцерогене ћелије – да производе до осам пута више интерферона-гама, кључног антитуморског сигналног протеина. То их је учинило ефикаснијим у убијању ХПВ-позитивних ћелија рака.
Код мишјих модела ХПВ-позитивног карцинома, вакцина је значајно успорила раст тумора. Поред тога, када је тестирана у узорцима тумора прикупљеним од ХПВ-позитивних пацијената са карциномом, вакцина на Н-крају је убила два до три пута више ћелија рака у поређењу са друга два дизајна вакцине.
„Овај ефекат није дошао од додавања нових састојака или повећања дозе. Дошао је од представљања истих компоненти на паметнији начин“, коаутор студије др Јоцхен Лорцхдиректор медицинске онкологије Нортхвестерн Медицине програма за рак главе и врата, рекао је у изјава.
„Имуни систем је осетљив на геометрију молекула“, рекао је он. „Оптимизирањем начина на који везујемо антиген на СНА, имуне ћелије су га ефикасније обрађивале.“
Гледајући унапред, коаутор студије Цхад Миркинпроналазач СНА и директор Међународног института за нанотехнологију Нортхвестерн-а, нада се да би овај приступ могао помоћи научницима да редизајнирају старије вакцине које су у почетку изгледале обећавајуће, али нису успјеле.
„Овај приступ је спреман да промени начин на који формулишемо вакцине“, рекао је Миркин у саопштењу. „Можда смо пропустили савршено прихватљиве компоненте вакцине само зато што су биле у погрешним конфигурацијама. Можемо се вратити на њих и реструктурирати их и трансформисати у моћне лекове.“
Овај чланак је само у информативне сврхе и није намењен пружању медицинских савета.
Хванг, Ј. ет ал. (2026). Постављање и оријентација Е711-19 диктирају ЦД8+ Т ћелијски одговор у структурно дефинисаним сферним вакцинама нуклеинских киселина. Сциенце Адванцес, 12(7). хттпс://дои.орг/10.1126/сциадв.аец3876