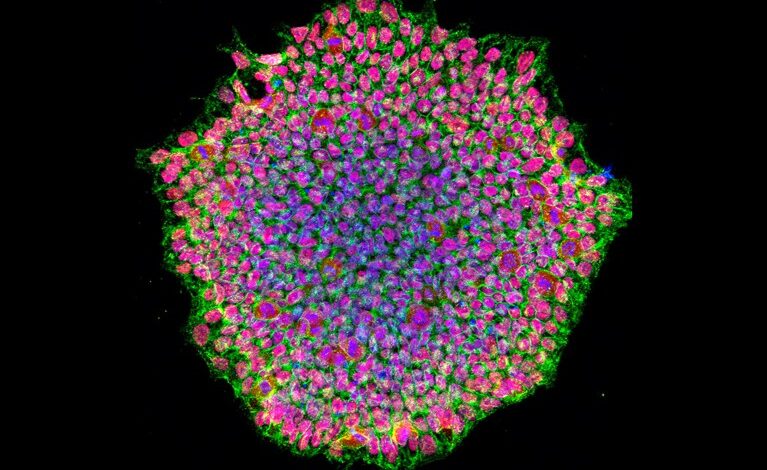
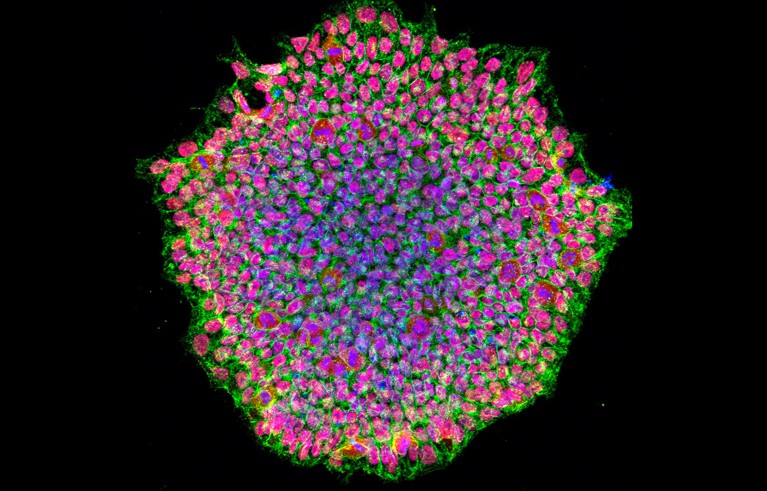
Третмани укључују репрограмирање зрелих ћелија у индуковане плурипотентне матичне (иПС) ћелије, затим прогениторске ћелије.Заслуге: Натионал Еие Институте/НИХ/Сциенце Пхото Либрари
Јапанско министарство здравља одобрило је издавање условног одобрења за два прва лека у врсти. Али неки истраживачи кажу да терапије – направљене од репрограмираних матичних ћелија и назване Амцхепри и РеХеарт – још нису спремне за ударно време.
„Ово је ризичан регулаторни експеримент“, каже Пол Кноепфлер, истраживач матичних ћелија на Калифорнијском универзитету у Дејвису.
Амчепри, који су јапанске фирме Сумитомо Пхарма и Рацтхера из Токија направили за лечење Паркинсонове болести, тестиран је на седам особа. РеХеарт, који је направио Цуорипс у Токију за тешку срчану инсуфицијенцију, тестиран је на осам људи. Али потребна су већа испитивања како би се осигурало да су ови лекови сигурни и ефикасни, каже Кноепфлер.
„Подаци које сам видео о овим производима изгледају охрабрујуће, али се чини да је рано да се прича о комерцијализацији таквих производа“, каже он.
Репрограмиране ћелије
Истраживачи регенеративне медицине већ дуго имају за циљ да користе матичне ћелије за узгој заменских ћелија за лечење низа болести.
Ове наде су добиле подстицај 2006. године, када су Шиња Јаманака и Казутоши Такахаши са Универзитета Кјото открили једноставан рецепт1 за репрограмирање зрелих ћелија у индуковане плурипотентне матичне ћелије. Техника је обезбедила нови извор ћелија које се могу трансформисати у друге типове ћелија. Јаманака је поделио Нобелову награду за своју улогу у делу 2012.

Велика опклада Јапана на терапије матичним ћелијама могла би се ускоро исплатити са револуционарним терапијама
Истраживачи из Сумитомо и Рацтхера користили су овај приступ да развију третман за Паркинсонову болест, неуродегенеративно стање које је узроковано губитком неурона у мозгу који производе допамин. Третман укључује прикупљање крвних зрнаца од добровољаца, њихово репрограмирање у ћелије познате као индуковане плурипотентне матичне (иПС) ћелије, затим наговарање репрограмираних ћелија да постану прогениторне ћелије које праве допамин. Неурохирурзи су затим тестирали технику пресађивањем ових ћелија у мозак људи са Паркинсоновом болешћу.
Амцхепри је сада тестиран у малој фази И/ИИ испитивања, која је дизајнирана углавном да процени безбедност. Нису се десили озбиљни нежељени ефекти, известили су истраживачи 20252. Најмање четири пацијента су показала смањење неких симптома, као што је тремор.
РеХеарт је такође направљен од ИПС ћелија добијених добровољцима, али се оне уместо тога диференцирају у ћелије срчаног мишића, а затим израстају у делове у облику новчића до 100 милиона ћелије. Они се пресађују у срца људи са врстом срчане болести која се зове исхемијска кардиомиопатија како би се подстакла кардиоваскуларна поправка.
У малој фази И суђења, РеХеарт се чинио безбедним, известили су истражитељи прошле године Америчко удружење за торакалну хирургију (ААТС), и показао је знаке помоћи неким пацијентима да постану физички активнији.
Пребацивање одговорности
За Хирошија Кавагучија, ортопедског хирурга у болници Надогаја у Чиби, Јапан, клинички подаци за оба лека су „веома слаби“. Ни једно испитивање није било довољно велико да процени ризике ових терапија, каже он. У испитивањима су такође недостајале контролне групе, што је онемогућавало чврсте закључке о томе колику корист пружају – ако их има.
Када су истраживачи представили РеХеарт податке ААТС-у, један члан публике је изразио сличне забринутости. „Потребно је да имате двоструко слепо контролисано суђење да бисте све убедили“, рекао је он.
Не журите са обећавајућим терапијама матичним ћелијама
У Јапану, међутим, регенеративни лекови који су прошли кроз истраживачка клиничка испитивања могу да обезбеде „условна и временски ограничена” одобрења. Комисија стручњака за министарство здравља препоручила је оба лека за ову врсту одобрења, за које се очекује да ће бити одобрено већ у марту.
Произвођачи лекова, осигуравачи и здравствени радници ће затим утврдити цену за производе, коју ће платити осигуравачи и пацијенти. Компаније тада могу да продају своје лекове током седам година ограниченом броју пацијената, а за то време ће наставити да прате како људи реагују да би боље проценили безбедност и ефикасност.